El laboratorio de Métodos Electrométricos forma parte del Departamento de Química Analítica y Aplicada de IQS. Una de sus principales actividades es el desarrollo de sensores de hidrógeno y litio para aplicaciones de alta temperatura.
En el marco del proyecto FusionCAT, el primer objetivo de la participación de IQS es el desarrollo de prototipos de sensores electroquímicos de hidrógeno capaces de operar en entornos químicos agresivos, como los reactores de fusión. Estas sondas son el primer paso hacia el desarrollo de sensores de tritio.
Los sensores electroquímicos pertenecen a la familia de sensores químicos. Los sensores químicos son dispositivos que convierten la información química (concentración o presión parcial del analito) en una señal medible. Los sensores electroquímicos presentan algunas ventajas frente a otros tipos de sensores químicos, como un procedimiento de medición simple, alta sensibilidad, tiempo de respuesta corto y la facilidad para ser miniaturizados. Estas propiedades hacen que estas herramientas sean de gran interés para el control de procesos industriales.
Los sensores electroquímicos más comunes son los potenciométricos, que miden la diferencia de potencial (en V), los conductimétricos, que miden la conductividad (en S / cm) y los amperométricos, que miden la corriente electroquímica (en A). Los sensores amperométricos muestran una gran versatilidad porque su respuesta depende del voltaje aplicado y el área activa de los electrodos. La Figura 1 muestra el esquema de un sensor amperométrico.
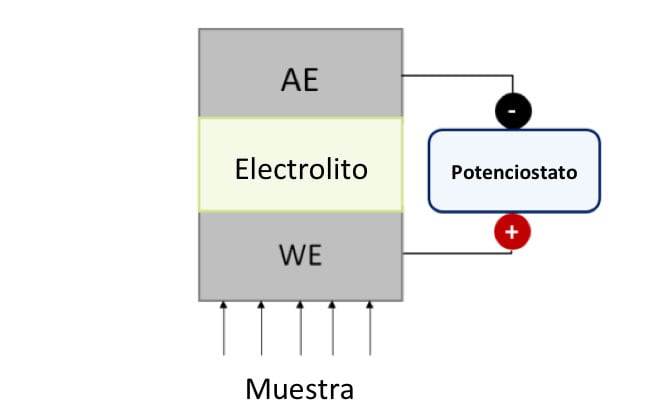
Figura 1. Representación esquemática de un sensor amperométrico genérico. WE: Electrodo de Trabajo, AE: Electrodo Auxiliar.
Los sensores amperométricos están compuestos por al menos dos electrodos: el de trabajo (WE) y el auxiliar (AE), que están en contacto a través de un electrolito común y conectados a un potenciostato. Inicialmente, el potenciostato aplica una diferencia de potencial. Posteriormente, el analito interactúa con el electrodo de trabajo y, finalmente, el potenciostato mide la corriente electroquímica asociada que fluye entre el WE y el AE. De esta forma se determina la concentración del analito.
A temperatura ambiente, estos dispositivos usan electrolitos en estado líquido, por lo que no pueden emplearse en aplicaciones a alta temperatura como son los reactores de fusión nuclear. En estos casos es necesario utilizar electrolitos en estado sólido. A pesar de que estos materiales sean sólidos, pueden transportar iones a través de su estructura cristalina. Por lo tanto, los electrolitos en estado sólido conductores de protón pueden ser utilizados para desarrollar sensores de hidrógeno de alta temperatura y, posteriormente, sensores de tritio.
En proyectos anteriores, se seleccionaron las cerámicas conductoras de protón BaCe0.6Zr0.3Y0.1O3-α y Sr(Ce0.9Zr0.1)0.95Yb0.05O3-α para la construcción de sensores. Estas cerámicas son perovskitas y presentan una buena conductividad de protones entre 400 y 1000°C.
Los sensores para experimentos de laboratorio se construyen uniendo un disco de estas cerámicas a un tubo de alúmina. Ambos lados del disco están metalizados con pintura de platino. De esta forma, la parte exterior del sensor actúa como electrodo de trabajo (ánodo) y la parte interior como electrodo auxiliar (cátodo). La Figura 2 muestra una representación esquemática de estos sensores y la Figura 3 muestra uno de los dispositivos experimentales utilizados.
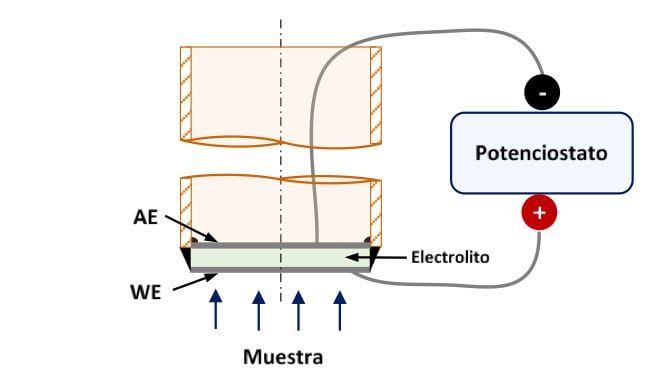
Figura 2. Esquema de un sensor de hidrógeno de alta temperatura para experimentos de laboratorio. WE: Electrodo de trabajo, AE: Electrodo auxiliar.
Cuando se aplica una diferencia de potencial entre ambos electrodos, el hidrógeno, que se encuentra en el electrodo de trabajo, se oxida para generar protones que se transportan a través del electrolito hasta el AE, donde se reducen para producir de nuevo hidrógeno. Por tanto, la corriente electroquímica asociada a este proceso es función de la concentración de hidrógeno en el electrodo de trabajo. Esta concentración de hidrógeno se determina mediante una recta de calibrado, obtenida previamente.
La corriente electroquímica depende del área activa de los electrodos. Cuanto mayor sea el área, mayor serán tanto la corriente como la sensibilidad. Otras geometrías, como tubos cerrados por un extremo, tienen áreas superficiales mayores que los discos utilizados para experimentos de laboratorio, por lo que la respuesta electroquímica de la sonda se puede mejorar cambiando su geometría. La Figura 4 muestra una representación de un sensor prototipo que usa un tubo cerrado por un extremo como electrolito.
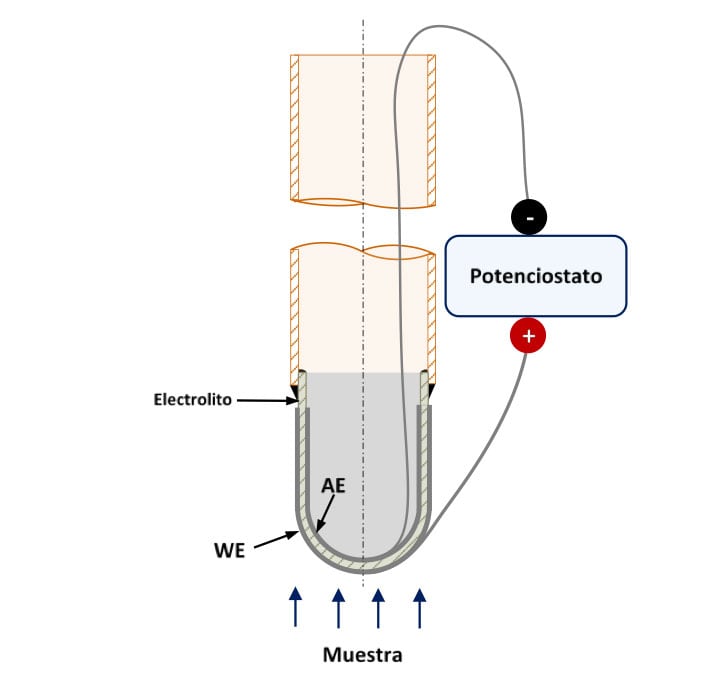
Figura 4. Representación esquemática de un prototipo de sensor de hidrógeno de alta temperatura que utiliza un electrolito de estado sólido en forma de tubo cerrado por un extremo. WE: Electrodo de trabajo, AE: Electrodo auxiliar.
Esta geometría se puede fabricar utilizando procesos de fabricación clásicos, como el slip casting, o desarrollados más recientemente, como el Spark Plasma Sintering (SPS) o la impresión 3D. Para este proyecto, es necesario fabricar pequeños lotes de estos componentes, por lo que la aplicación de estos nuevos procesos de fabricación contribuirá al éxito de este hito del proyecto.


